Europio, o símbolo é Eu e o número atómico é 63. Como membro típico dos lantánidos, o europio adoita ter unha valencia de +3, pero tamén é común unha valencia de osíxeno de +2. Hai menos compostos de europio cun estado de valencia de +2. En comparación con outros metais pesados, o europio non ten efectos biolóxicos significativos e é relativamente non tóxico. A maioría das aplicacións do europio empregan o efecto de fosforescencia dos compostos de europio. O europio é un dos elementos menos abundantes no universo; só hai uns 5 no universo × 10-8 % da substancia é europio.
O europio existe na monacita
O descubrimento do europio
A historia comeza a finais do século XIX: naquel momento, excelentes científicos comezaron a cubrir sistematicamente as vacantes restantes na táboa periódica de Mendeleev analizando o espectro de emisión atómica. Desde o punto de vista actual, este traballo non é difícil e un estudante universitario pode completalo; pero naquel momento, os científicos só tiñan instrumentos de baixa precisión e mostras difíciles de purificar. Polo tanto, en toda a historia do descubrimento dos lantánidos, todos os descubridores "cuasi" seguiron facendo afirmacións falsas e discutindo entre si.
En 1885, Sir William Crookes descubriu o primeiro sinal, aínda que non moi claro, do elemento 63: observou unha liña espectral vermella específica (609 nm) nunha mostra de samario. Entre 1892 e 1893, o descubridor do galio, o samario e o disprosio, Paul émile LeCoq de Boisbaudran, confirmou esta banda e descubriu outra banda verde (535 nm).
A continuación, en 1896, Eugène Anatole Demarçay separou pacientemente o óxido de samario e confirmou o descubrimento dun novo elemento de terras raras situado entre o samario e o gadolinio. Separou con éxito este elemento en 1901, marcando o final da viaxe de descubrimento: «Espero chamar a este novo elemento europio, co símbolo Eu e unha masa atómica de aproximadamente 151».
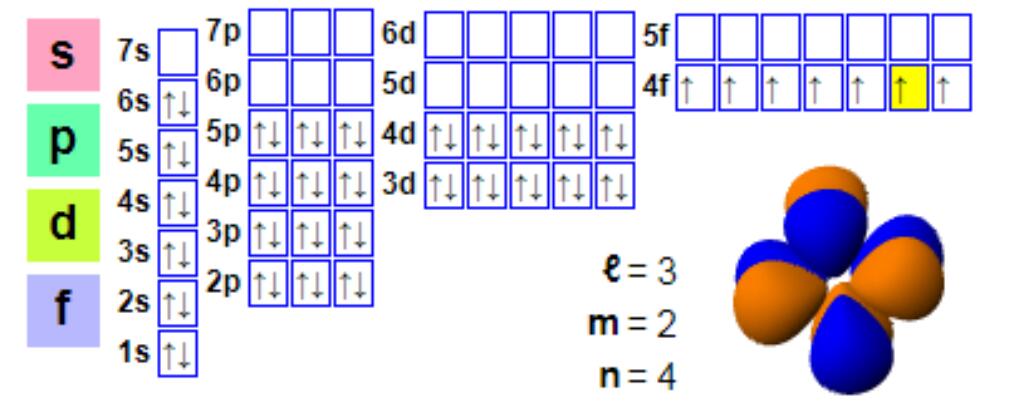
Configuración electrónica
Configuración electrónica:
1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 5p66s2 4f7
Aínda que o europio adoita ser trivalente, é propenso a formar compostos divalentes. Este fenómeno é diferente da formación de compostos de valencia +3 pola maioría dos lantánidos. O europio divalente ten unha configuración electrónica de 4f7, xa que a capa f semichea proporciona máis estabilidade, e o europio (II) e o bario (II) son similares. O europio divalente é un axente redutor suave que se oxida no aire para formar un composto de europio (III). En condicións anaeróbicas, especialmente condicións de quecemento, o europio divalente é suficientemente estable e tende a incorporarse ao calcio e outros minerais alcalinotérreos. Este proceso de intercambio iónico é a base da "anomalía negativa do europio", é dicir, en comparación coa abundancia de condrita, moitos minerais lantánidos como a monacita teñen un baixo contido de europio. En comparación coa monacita, a bastnaesita adoita presentar menos anomalías negativas de europio, polo que a bastnaesita tamén é a principal fonte de europio.
O europio é un metal de cor gris ferroso cun punto de fusión de 822 °C, un punto de ebulición de 1597 °C e unha densidade de 5,2434 g/cm³. É o elemento menos denso, máis brando e máis volátil entre os elementos de terras raras. O europio é o metal máis activo entre os elementos de terras raras: á temperatura ambiente, perde inmediatamente o seu brillo metálico no aire e oxídase rapidamente en po; reacciona violentamente con auga fría para xerar gas hidróxeno; o europio pode reaccionar con boro, carbono, xofre, fósforo, hidróxeno, nitróxeno, etc.
Aplicación do europio
O sulfato de europio emite fluorescencia vermella baixo luz ultravioleta
Georges Urbain, un xoven químico destacado, herdou o instrumento de espectroscopia de Demarçay e descubriu que unha mostra de óxido de itrio(III) dopada con europio emitía unha luz vermella moi brillante en 1906. Este é o comezo da longa viaxe dos materiais fosforescentes de europio, que non só se usan para emitir luz vermella, senón tamén luz azul, porque o espectro de emisión do Eu2+ está dentro deste rango.
Un fósforo composto de emisores vermellos Eu3+, verdes Tb3+ e azuis Eu2+, ou unha combinación deles, pode converter a luz ultravioleta en luz visible. Estes materiais desempeñan un papel importante en varios instrumentos de todo o mundo: pantallas intensificadoras de raios X, tubos de raios catódicos ou pantallas de plasma, así como nas recentes lámpadas fluorescentes de aforro de enerxía e díodos emisores de luz.
O efecto de fluorescencia do europio trivalente tamén pode ser sensibilizado por moléculas aromáticas orgánicas, e tales complexos poden aplicarse en diversas situacións que requiren unha alta sensibilidade, como tintas e códigos de barras anticorrupción.
Desde a década de 1980, o europio desempeñou un papel destacado na análise biofarmacéutica de alta sensibilidade mediante o método de fluorescencia fría con resolución temporal. Na maioría dos hospitais e laboratorios médicos, esta análise converteuse en rutina. Na investigación das ciencias da vida, incluída a imaxe biolóxica, as sondas biolóxicas fluorescentes feitas de europio e outros lantánidos son omnipresentes. Afortunadamente, un quilogramo de europio é suficiente para soportar aproximadamente mil millóns de análises; despois de que o goberno chinés restrinxise recentemente as exportacións de terras raras, os países industrializados atemorizados pola escaseza de almacenamento de elementos de terras raras non teñen que preocuparse por ameazas similares a tales aplicacións.
O óxido de europio utilízase como fósforo de emisión estimulada en novos sistemas de diagnóstico médico de raios X. O óxido de europio tamén se pode usar para fabricar lentes de cores e filtros optoelectrónicos, para dispositivos de almacenamento de burbullas magnéticas e en materiais de control, materiais de blindaxe e materiais estruturais de reactores atómicos. Debido a que os seus átomos poden absorber máis neutróns que calquera outro elemento, úsase habitualmente como material para absorber neutróns en reactores atómicos.
No mundo actual en rápida expansión, a aplicación recentemente descuberta do europio pode ter un profundo impacto na agricultura. Os científicos descubriron que os plásticos dopados con europio divalente e cobre univalente poden converter eficientemente a parte ultravioleta da luz solar en luz visible. Este proceso é bastante ecolóxico (son as cores complementarias do vermello). Empregar este tipo de plástico para construír un invernadoiro pode permitir que as plantas absorban máis luz visible e aumenten o rendemento das colleitas nun 10 % aproximadamente.
O europio tamén se pode aplicar a chips de memoria cuántica, que poden almacenar información de forma fiable durante varios días seguidos. Estes poden permitir que os datos cuánticos sensibles se almacenen nun dispositivo similar a un disco duro e se envíen a todo o país.
Data de publicación: 27 de xuño de 2023